妇科医生王继东博士的科普号
- 精选 单孔之美,术后无痕:经阴道单孔腹腔镜手术
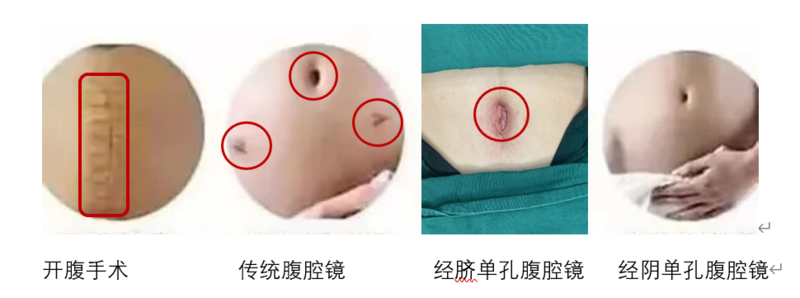
爱美之心,人皆有之。当需要通过手术解除病痛的情况下,手术疤痕是无法越过去的坎儿。谁都不想在自己完美无瑕的肌肤上留下疤痕。妇科手术发展至今天,从最初的开腹手术,到后来的传统腹腔镜手术,再到今天的单孔腹腔镜手术,正在以越来越微创的技术理念满足爱美女士的需求。通过下图我们来比较开腹手术、传统腹腔镜手术、经脐单孔腹腔镜以及经阴道单孔腹腔镜手术伤口的区别。开腹手术:手术切口大,术后疤痕明显。传统腹腔镜:3-4个小疤痕,疤痕不明显经脐单孔腹腔镜:只在脐部有一个疤痕,肚脐可以遮挡,疤痕几乎不可见。经阴道单孔腹腔镜:手术切口在阴道,术后愈合良好。腹部完美无痕。单孔腹腔镜手术是指通过1个切口进入人体,置入腹腔镜器械进行的手术操作。常规的腹腔镜手术需要在人体做3-5个切口,可以看作是多孔腹腔镜。根据入路的不同,单孔腹腔镜可分为经自然腔道的腹腔镜手术和经脐单孔腹腔镜手术。经脐单孔腹腔镜是在肚脐部位做一个2-3cm的切口,置入腹腔镜的器械完成操作的手术技术。之所以选择肚脐作为手术入路,是因为肚脐是人体唯一一个天然的疤痕结构。在这里进行手术不会增加额外的疤痕,通过肚脐的天然凹陷可以遮盖手术疤痕,有利于美观。优势在于:创伤小、痛苦少、恢复快、易于取标本、较强的美容效果。手术切口选择在阴道最深处,打开阴道后穹窿或前穹窿3-4厘米的切口,置入腹腔镜的器械完成手术操作。这是最近几年兴起的妇科手术的入路,从阴道这个自然腔道操作,手术疤痕隐藏在阴道深处的皱褶内,术后几乎无痕迹,而且对肠道干扰小,术后肠功能恢复快,由于阴道上段神经分布特点,术后疼痛明显较经腹部手术轻,是将来微创手术的一个发展方向。山东省妇幼保健院妇科肿瘤综合诊治中心目前熟练开展经阴道单孔腹腔镜手术,可以完成子宫切除术、输卵管妊娠手术(输卵管切除术、输卵管开窗取胚术)、卵巢切除术、卵巢囊肿剥除术等手术。结合术后快速康复理念,本中心以患者以更小的创伤,更轻的疼痛、更快的康复,更好的就诊体验为服务宗旨,为您的健康保驾护航。
 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1408人已读
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1408人已读 - 视频 输卵管导丝疏通手术
 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心625人已观看
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心625人已观看 - 精选 带你了解真实的子宫肌瘤长什么样
 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1895人已观看
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1895人已观看 - 精选 三种hpv疫苗哪种更好?
HPV疫苗目前有二价、四价和九价三种。有人觉得价别越高越好。其实从目前的数据和观察结果来看,从预防宫颈癌角度,三种疫苗是一样有效的,都可以达到90%以上。从疫苗可及性角度,二价疫苗就是很好的选择。 四价疫苗和二价疫苗相比,多了两种尖锐湿疣的hpv型别。也就是说四价可以预防尖锐湿疣,而二价不可以。 另外,三种疫苗不推荐混着打。
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心7142人已读 - 精选 宫颈囊肿需要治疗吗
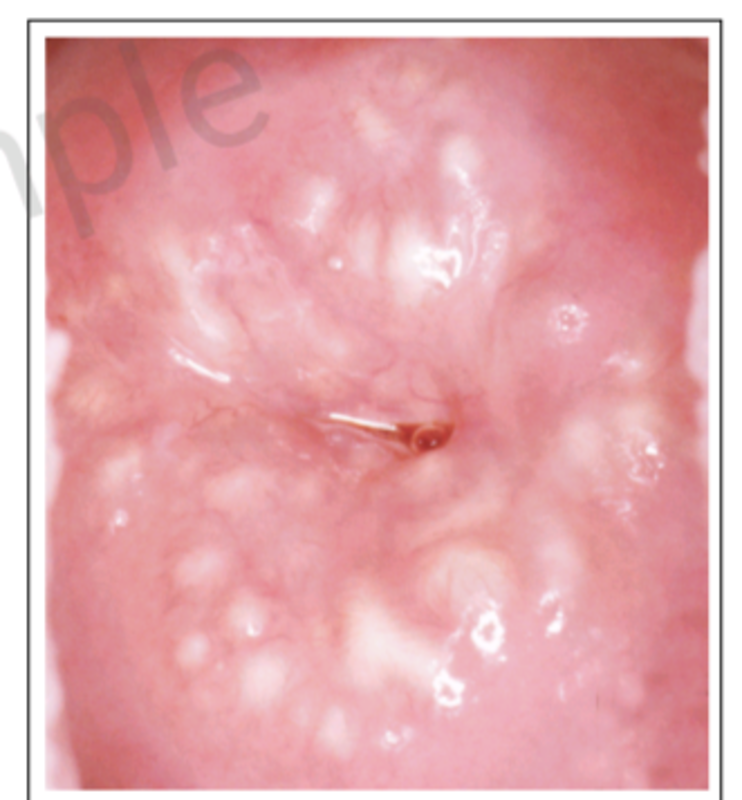
宫颈囊肿是怎么形成的很多人在妇科检查或盆腔B超检查后被告知有"宫颈囊肿",就以为自己得了肿瘤,是很严重的病。其实,宫颈囊肿和肿瘤完全是两码事。 我们知道,宫颈上是有腺体的。什么是腺体,就是具有分泌功能的一种结构,例如汗液是由汗腺分泌,泪水由泪腺分泌的。宫颈上的腺体分泌的是一种透明的粘液。腺体是有开口的。当宫颈腺体开口被堵塞,腺体分泌的粘液不能流出就积聚在腺腔内,越积越大,就形成了所谓的“宫颈囊肿” 宫颈囊肿是不需要治疗的因此,宫颈囊肿并非是什么肿瘤,也没有必要乱担心了。如果长得很大可以刺破让囊肿内的液体流出来,但可能还会再长。 虽然宫颈囊肿是不需要治疗的,但它可能和宫颈的其他病变同时存在,因此规范的宫颈检查如宫颈癌筛查,还是要做的。如果发现有宫颈癌前病变,需要规范的治疗。
 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1.6万人已读
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心1.6万人已读 - 精选 HPV致癌蛋白E6/E7诱导细胞恶变的分子机制
引言在所有人类癌症中,5%的恶性肿瘤发病都与人乳头瘤病毒(HPVs)有关,而宫颈癌和HPV是关系最密切的。E6/E7两种病毒蛋白对于恶性肿瘤的发展和维持是至关重要的。维持细胞稳态的关键通路是这两种蛋白主要的作用位点。它们对细胞作用的结果是营造一个有利于病毒存活的环境;但是当受到干扰时就会导致对宿主细胞的改变,最终导致恶性肿瘤的发生发展。 简介HPVs是一种小型的双链DNA病毒,特异性感染上皮细胞。HPV家族包含约200种病毒亚型。每种病毒亚型的组织特异性是不同的。大多数的HPV亚型引起的病变均为良性的,具有自限性;只有少部分病毒为高危亚型,可以引起人类的恶性肿瘤。这些肿瘤包括宫颈癌,肛门生殖器以及头颈部肿瘤。HPV高危亚型有其独特的生物学特性,他们能够干扰宿主对细胞增殖和基因组稳定的调控能力。几乎所有的宫颈癌(>99%)都与高危HPV感染有关。HPV感染的最初几个月,患者是没有任何症状的,并且大约90%的感染会在2年内通过宿主的免疫系统清除。只有那些不能通过免疫系统清除的高危HPV持续性感染,才会导致宫颈癌的发生。HPV16,18是导致宫颈癌的最常见亚型,全球80%宫颈癌发病都与他们有关。其他高危亚型包括31, 33, 35, 39, 45, 51, 52, 56, 58和59。 HPV诱导癌变的特征之一,即表现为E6/E7两种病毒蛋白的持续表达,贯穿于肿瘤发生的全程,并维持癌症表型。如果抑制E6和或E7的表达和功能,肿瘤细胞的增殖停滞并发生凋亡。因此,他们是治疗HPV诱导的恶变的理想靶点。 HPV生命周期:从感染到恶变的演进 HPV生命周期与宿主上皮细胞的分化密切相关。复层鳞状上皮因为微小损伤导致基底层暴漏,HPV感染基底层细胞。HPV生命周期由此开始,因为只有基底层细胞是具有增殖能力的。HPV感染宿主细胞后,以染色体外元件或附加体的形式构建基因组,依靠细胞复制蛋白调节病毒DNA合成。HPV感染过程中,非基底层细胞大部分处于正常的细胞周期,而一小部分细胞重新进入S期完成HPV病毒基因组的扩增。与此同时,病毒衣壳蛋白及病毒体组装随之完成,最终具有感染性的病毒颗粒被释放出来。E6/E7蛋白与细胞周期调控因子(pRb蛋白,E2F转录因子,P53等)相互作用,细胞周期节点(chekpoints)被废除,最终导致感染细胞的“永生”。由于E6/E7蛋白干扰细胞正常周期,导致细胞不断合成DNA,DNA损伤监控失控,很容易引起突变的发生。突变可以是点突变,也可以是大段染色体突变。HPV感染宫颈细胞,一般情况下出现程度较轻的细胞异常,组织学上表现为宫颈上皮内瘤变(CIN1-2)。这种程度的病变伴随着免疫系统对病毒的清除可以在1-2年内消退。然而HPV有多种机制可以抵抗免疫系统,即免疫逃避,从而导致宿主细胞的持续性感染,最终形成宫颈癌。 在低级别病变中,HPV以游离体的状态存在于宿主细胞中;而在高级别病变中,其基因组是整合到宿主细胞染色体内的。目前这些整合位点还没有被识别,但引起基因组不稳定的脆弱位点已经被发现。近年研究发现,在宿主细胞染色体的脆弱位点有HPV基因组的复制,并“劫持”宿主的DNA损伤应答,病毒整合到这些位点的几率增加,反过来进一步促进这些区域的DNA重组。HPV诱导细胞恶变过程中病毒基因组整合的精确作用存在争论,似乎与E6/E7的表达失控有关。维持宫颈癌细胞株持续增殖的必要条件是E6/E7蛋白的持续表达。众多实验通过抑制E6/E7的表达,获得了这方面的证据。 E6/E7的分子靶点E6蛋白有众多的与其相互作用的伴侣蛋白;这些蛋白有不同的生物学功能。其中P53肿瘤抑制因子是最重要的一个。E6蛋白与泛素连接酶结合使其维持稳定状态,再与P53蛋白结合形成三聚体,使P53蛋白发生多聚泛素化,失去了对细胞生长、凋亡和DNA 修复的调控作用。E6蛋白的这种作用一般只见于高危HPV。E6的靶蛋白均具有一个共同的α螺旋结构,调节E6与泛素连接酶的结合。因此,如果对α螺旋结构进行干预,势必会影响E6蛋白的多种生物学功能。目前还无法明确每个伴侣蛋白与 E6结合后发挥的具体生物学作用。低危HPV的E6蛋白虽然也与P53相互作用,但主要对病毒生命周期发挥作用,而不会诱导癌变。高危HPV亚型E6蛋白的羧基端有一段特殊的氨基酸,可以与细胞内的一组特异蛋白结合,这被认为是其致癌潜能的标志。而这种结构在低危HPV亚型的E6蛋白中是缺失的。与E6蛋白特殊结构域结合的细胞蛋白均具有重要的生物学功能,例如细胞粘附、细胞链接以及细胞极化等。E6蛋白与这些细胞蛋白结合,使细胞更具有侵袭性,或者可以使E6维持高表达。 和E6蛋白类似,E7蛋白可以和伴侣蛋白结合发挥多种生物学功能和活性。高危HPV亚型的E7蛋白最重要的结合靶点是肿瘤抑制因子pRB蛋白,在cullin 2泛素化连接酶介导下,使pRB蛋白功能失控。E7蛋白还可以通过调节细胞周期蛋白激酶从而使细胞周期失调控。 E6/E7蛋白对DNA损伤应答、表观遗传调控的作用HPV表达的E6/E7蛋白不能直接将正常细胞转化为癌细胞。他们可以使宿主细胞发生基因组不稳定性,而后者正是细胞恶变的必要条件。宿主细胞染色体出现单倍体、三倍体、双微小体等异常均与E6/E7蛋白的表达有关。使细胞发生基因组不稳定是E6/E7蛋白诱发癌变的早期事件,早于其基因组整合入宿主细胞染色体。有研究发现宫颈癌的癌前病变中存在染色体非整倍体现象,这与前面的理论不谋而合。而在低危HPV感染的细胞中却没有这种现象。另外,高危E6/E7蛋白的表达使有丝分裂缺陷出现,包括多极有丝分裂、后期桥体、非整倍体等。多极有丝分裂常与异常中心体数目、核异型共同存在。研究表明,异常的中心体扩增是基因组不稳定的早期变化。E7蛋白使细胞在单一的S期内发生多次中心体合成,而这些中心体是由一个母系中心粒转变而来,具有不成熟性。正常情况下,出现异常有丝分裂会导致细胞死亡;而E6/E7的协同作用让细胞携带这些异常有丝分裂而继续存活,最终结果是多倍体细胞的不断积累增多。过度生长的异常细胞最终导致癌变的发生。 E6/E7蛋白的表达,通过抑制P53功能使细胞正常的DNA损伤应答失活;它们都可以独立的诱导细胞DNA损伤,增加了HPV基因组整合入宿主细胞基因组的几率。宿主细胞DNA损伤修复功能也出现异常,是有缺陷的损伤修复。DNA损伤应答的异常导致细胞基因组不稳定性的出现,最终导致癌变的发生。 HPV的致癌作用高危E6/E7蛋白可以影响细胞多个调节通路,并通过多种方式打乱细胞内稳态的环境。使宿主细胞发生癌变的另一个重要因素就是感染时间长短。一个完整的病毒生命周期需要2-3周,只有在足够长的感染时间内宿主细胞的基因发生改变,进而才会促使细胞恶变。目前研究的一个热点问题是HPV感染的宿主细胞是否具有干细胞的特点。宫颈转化区的干细胞或储备细胞是HPV感染的主要宿主细胞。HPV感染使宫颈转化区细胞形成不典型增生是HPV感染长期潜伏的基础,尤其是宫颈鳞-柱交接部的细胞,与HPV相关的宫颈癌发生有主要关系。鳞-柱交接部的细胞为胚胎起源,是一种单层的立方上皮,其基因表达系统不同于转化区其他位置的宫颈细胞。在宫颈CIN病变和宫颈癌中发现一些特殊蛋白,体外的鳞状上皮细胞E6/E7不能诱导这些蛋白表达,尤其当宫颈鳞-柱交接部的组织通过锥切或leep手术切除后,这些蛋白的表达缺失。 有学者正在寻找鉴别宫颈干细胞的方法,有研究发现CD66+的细胞具有恶变潜能。虽然宫颈干细胞的假说证据有限,但还是比较令人信服的。“宫颈干细胞”、“储备细胞”以及鳞柱交接部细胞和宫颈癌发生的关系,是当前宫颈癌研究的热点。肿瘤细胞的异质性是临床治疗的巨大挑战,继续寻找这些细胞的标志性特点成为治疗的新靶点是未来研究的方向。 结论综上,E6/E7蛋白在HPV相关恶性肿瘤中具有重要作用。方兴未艾的“组学”技术以及个体化医疗,给我们临床治疗恶性肿瘤提供了新的方向。随着对E6/E7蛋白诱导HPV相关癌症的分子机制研究的不断深入,其可能会成为临床宫颈癌治疗的新靶点。 文献来源: 1.Suruchi Mittal, Lawrence Banks, Molecular mechanisms underlying human papillomavirus E6 and E7 oncoproteininduced cell transformation, Mutation Research-Reviews in Mutation Research. http://dx.doi.org/10.1016/j.mrrev. 2016.08.001 2.Julia Durzynska, Krzysztof Lesniewicz, Elzbieta Poreb, Human papillomaviruses in epigenetic regulations, Mutation Research 772 (2017) 36–50. http://dx.doi.org/10.1016/j.mrrev.2016.09.006
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心8077人已读 - 视频 山东省妇幼保健院妇科肿瘤中心
 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心38人已观看
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心38人已观看 - 典型病例 巨大卵巢囊肿——单孔腹腔镜手术安排上!
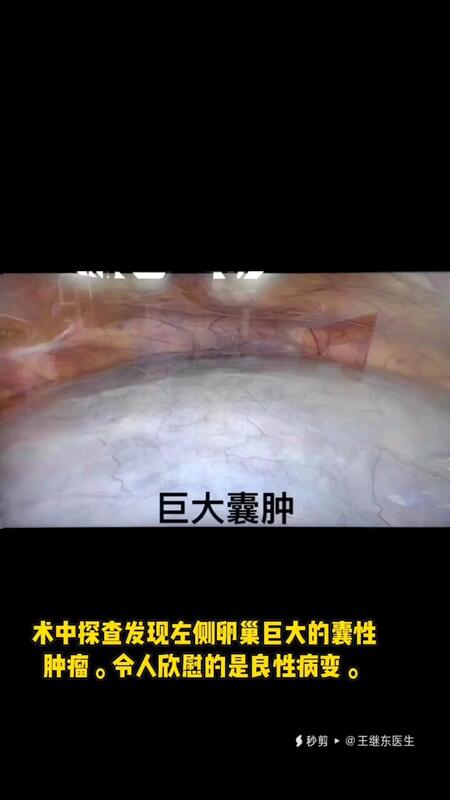 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心63人已观看
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心63人已观看 - 医学科普 单孔腹腔镜完美解决子宫肌瘤,更微创更美观。
单孔腹腔镜和传统腹腔镜手术不同之处,主要在于只在肚脐做一个小切口,就可以完成手术。手术更加微创,术后几乎看不到腹壁瘢痕。看一个刚出院不久的实际病例。
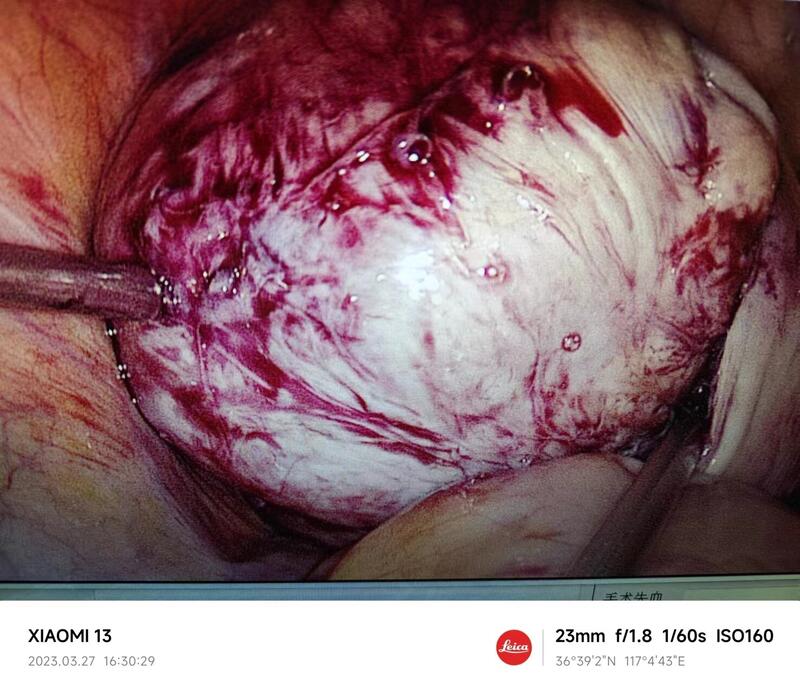 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心98人已读
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心98人已读 - 医学科普 腹腔镜下宫颈环扎术:治疗宫颈机能不全有明显优势
宫颈机能不全唯一有效的治疗办法就是宫颈环扎术。其原理可以简单理解为,用带子(环扎带)把子宫这个口袋的口紧紧地扎住。宫颈环扎术分经阴道环扎和经腹环扎。经阴环扎手术,一般选择在怀孕16周左右完成手术。优点是操作相对简单,环扎带拆除方便,缺点是环扎效果相对差,有些患者在手术后为了保证效果,不能自由活动,在床上待到分娩。经腹环扎手术,一般在怀孕前完成,或者在怀孕10周左右做手术。主要通过腹腔镜微创手术实施。优点是环扎更牢靠,分娩时可以不拆除环扎带,下次怀孕继续用。缺点是分娩要采取剖宫产方式,怀孕中晚期如果发现胎儿异常,引产前可能需要先拆除环扎带。这是一例宫颈环扎术患者术中照片。患者住院四天,当天下床活动,疼痛轻微。腹腔镜宫颈环扎术,患者创伤小恢复快,环扎效果稳定。
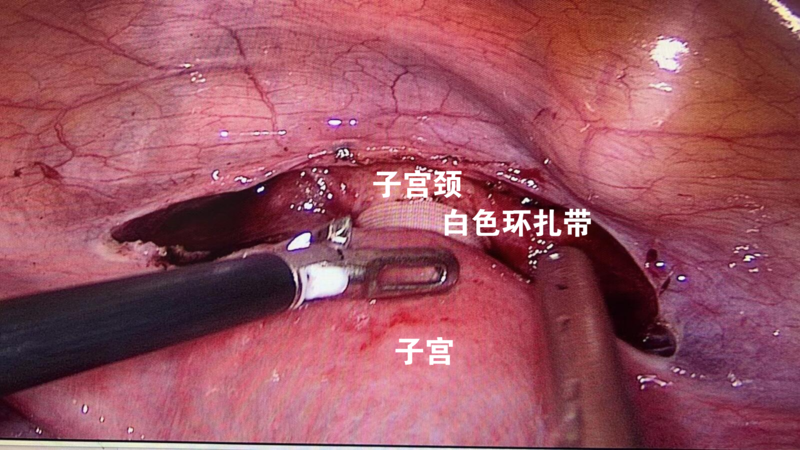 王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心189人已读
王继东 副主任医师 山东省妇幼保健院 妇科肿瘤综合诊治中心189人已读





